Les perspectives thérapeutiques dans la polyarthrite rhumatoïde
- Détails
- Mis à jour le 19 juin 2012
Pr. Selma El Hassani
Service de rhumatologie. Hôpital Ibn Tofail. CHU Mohammed VI. Marrakech
07/12/2010
L'amélioration de la connaissance de l'immunopathologie de la polyarthrite rhumatoïde (PR) a ouvert de nouvelles perspectives thérapeutiques. En effet depuis quelques années se développe une immunothérapie sélective ou partiellement sélective utilisant des drogues dites ciblées ou biothérapie. Ces biothérapies agissent sur certaines cellules ou certains médiateurs biologiques dont on connaît le rôle lésionnel. La première voie explorée est celle des anti -TNF connaissant le rôle lésionnel du TNF alpha dans la PR. Mais rapidement on se rend compte que 30 à 40% des patients ne répondaient pas à l'anti-TNFalpha. A ce moment la recherche s'oriente vers d'autres pistes et voies d'exploration de l'inflammation dans la PR [1]. Selon la nouvelle conception physiopathologique de la PR cette pathologie inflammatoire est considérée comme une affection liée à un processus d'immunité cellulaire impliquant dans cette réaction le lymphocyte T B et la cellule présentatrice d'antigène (CPA) (fig : n° 1)[2]. Ce basant sur cette approche il existe plusieurs niveaux d'action médicamenteuse pour modifier ou moduler la réaction immunitaire. Il peut s'agir de thérapeutique modulant les cytokines des biothérapies dirigées contre les lymphocytes ou de biothérapie modulant l'interaction intercellulaire LT LB ou CPA.
1-MODULATION DES CYTOKINES :
Dans la PR il existe une rupture de l'équilibre entre les cytokines pro-inflammatoires et les cytokines anti-inflammatoires. Les cytokines inflammatoires vedettes sont : IL1 TNF alpha IL6 et bien d'autres. Nous développerons l'IL 1 et l'IL 6.
A -L'IL1 :
La sécrétion de l'IL1 peut être modulée de deux façons. En agissant sur le récepteur soluble de l'IL1 ou en agissant sur l'antagoniste de son récepteur. La première voie est rapidement abandonnée au profit du développement de l'anticorps monoclonal anti IL 1. Le produit est l'Anakinra. Le développement de la molécule débute en 2000 et la première étude portait sur un effectif de 472 patients atteints de PR ne répondant pas ou partiellement au Méthotrexate. Les patients recevaient 150 mg d'Anakinra. L'analyse à 24 semaines montre 43% de répondeurs ACR 20 contre 27% de répondeurs ACR 20 pour le placebo. D'autres études plus prolongées parfois (48 semaines) et sur des échantillons plus développés ne montrent qu'un effet moyen de la molécule [3]. Une deuxième ligne de protocoles s'oriente vers l'association de deux anti-cytokines. Il y a eu de ce fait des essais associant Anakinra et anti-TNF (Infliximab Etanercept). La comparaison Anakinra plus Etanercept et Etanercept seul donne des résultats en défaveur de l'Anakinra dans la mesure où les résultats en terme ACR50 sont en faveur du premier groupe Etanercept seul avec une augmentation des effets secondaires surtout infectieux [4]. Les résultats de cette association de biothérapie sont à l'origine d'une mise au point de recommandation de l'AFSSAPS mettant en garde et déconseillant l'association Anakinra Etanercept. (Voire encadré).
B - L'IL6 :
L'IL6 est une cytokine qui joue un rôle ubiquitaire et participe à la production d'anticorps à l'activation du lymphocyte T à la majoration de l'induction et surtout à l'accélération de l'inflammation. Le blocage du signal IL6 peut se faire de deux manières. Par blocage direct de l'IL 6 ou par inhibition du récepteur de l'IL6. La première voie fut rapidement abandonnée car paradoxalement l'anticorps bloquant l'IL6 donne une augmentation de la production de celle-ci. L'inhibition du récepteur se fait soit sur le récepteur soluble ou membranaire. Cet anticorps s'appelle MRA (fig : 2) [5]. Il est en développement par les laboratoires ROCHE. Deux principales études dans le développement de la molécule. Les deux utilisent 2 doses de MRA : 4 et 8 mg/kg. La première testant MRA en monothérapie et la deuxième en association avec le Méthotrexate. Les résultats sont intéressants en terme de réponse ACR 20 et ACR 50 pour la dose de 8mg/kg qui et retenu comme dose thérapeutique (fig :3). La tolérance du MRA est bonne dans les deux études. Les effets secondaires sont marquées par une augmentation réversible du cholestérol total cholestérol HDL et des transaminases avec des réactions anaphylactiques dans le groupe faible dose [6].
II / BIOTHERAPIE MODULANT L'INTERACTION INTERCELLULAIRE LT LB OU CPA
A – CTLA 4 :
Pour induire une réaction d'immunité par activation du lymphocyte T il faut que l'Ag soit présenté par le complexe d'histocompatibilité à la CPA. Ce point de contact entre les deux systèmes n'est pas suffisant pour déclencher la réponse immunitaire. Ainsi la liaison entre CD80 CD86 sur la CPA et CD28 sur le lymphocyte T participe au renforcement de la réaction immunitaire. Une molécule naturelle CTLA4 (cytotoxic T lymphocyte antigene4) inhibe cette liaison en se fixant sur le CD80 CD86 avec une grande affinité (fig :4) [5]. Cette molécule (CTLA4) est développée en thérapeutique. Elle a été couplée à un fragment Fc d'immunoglobuline pour augmenter sa durée de vie d'où le CTLA4-Ig ou Abatacept.
Les études du développement ont utilisés l'Abatacept chez des patients atteints de PR active sous Méthotrexate et ne répondant pas à ce traitement. Deux doses ont été utilisés : 2mg/kg et 10mg/kg. Les résultats à 24 semaines montrent avec la forte dose de bons résultats avec 60% de répondeurs ACR20 (fig :5) [1]. A 48 semaines l'action se maintient. La tolérance est bonne et particulièrement la tendance à l'infection notée avec l'anti-TNF ne représente pas le premier souci avec l'Abatacept. La deuxième étude avec l'Abatacept montre son effet structural à 10mg. En effet la molécule entraîne une freination de l'aggravation structurale avec un indice de sharp qui s'aggrave de 12 dans le bras Abatacept et Méthotrexate et de 232 dans le bras placebo [7].
La deuxième ligne d'essai concerne l'utilisation d'Abatacept dans la PR réfractaire aux anti-TNF. Les résultats sont intéressants avec une efficacité en terme d'ACR20 chez plus de 50% des malades. La tolérance est aussi bonne et particulièrement en ce qui concerne les complications infectieuses. Il n'y a pas de différences significatives entre Abatacept et placebo [8].
B -CD40-CD40 ligand
Les lymphocytes T activées expriment GP39 ou CD40 ligand qui est le ligand de CD40 présent sur plusieurs cellules : CPA et lymphocytes B. Le blocage du CD40 ligand par un anticorps peut exercer une activité immunosuppressive (fig:6). La molécule est en étude pré clinique. Elle a montré un effet préventif de l'arthrite au collagène de type II.
A coté de ces thérapeutiques d'autres cytokines et d'autres voies de recherches portent actuellement sur : Anti-IL15 Anti-IL17 l'Anti-Rank-L l'OPG et la liste et très longue.
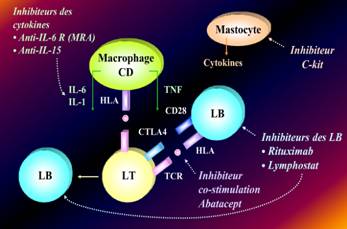
Figure n° 1 : Implication entre lymphocyte T B et la cellule présentatrice d’antigène (CPA)
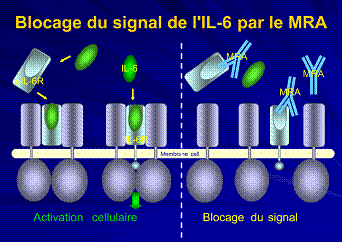
Figure n° 2: Blocage du signal de l’IL6 par MRA
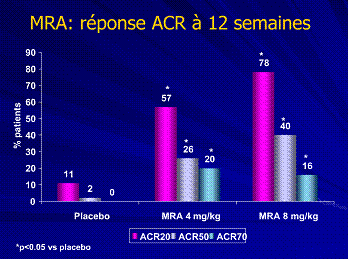
Figure 3 : Abatacept chez des patients atteints de PR active sous Méthotrexate. Réponse ACR 20 ACR 50 ; ACR 70
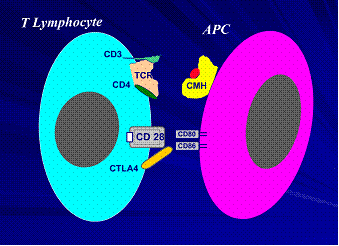
Figure n° 4 : Présentation de l’Ag par le complexe d’histocompatibilité à
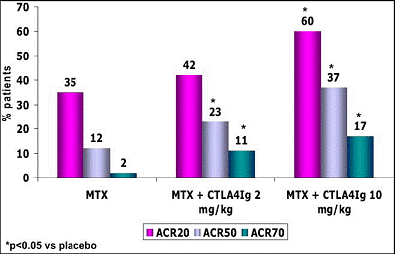
Figure 5 : évaluation du CTLA-Ig (ou Abatacept) en association au MTX à 24 semaines chez des patients atteints de PR active dans un essai contrôlé vs placebo.
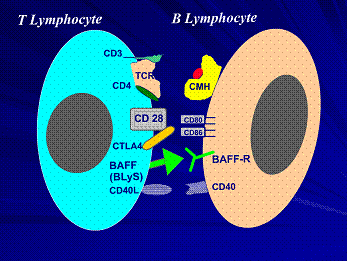
Figure 6 : Présentation de l’Ag par le complexe d’histocompatibilité à
1 / Xavier Mariette. Biothérapies émergentes dans la polyarthrite rhumatoïde. Rev Rhum 2004 ; 71:848–853.
2 / Jean Sibilia. SFR 2003.
3 / Dayer JM Feige U Edwards CK Burger D. Anti interleukin-1 therapy in rheumatic diseases. Curr Opin Rheumatol 2001;13:170–6.
4 / Genovese MC and all Combination therapy with etanercept and anakinra in the treatment of patients with rheumatoid arthritis who have been treated unsuccessfully with methotrexate. Arthritis Rheum. 2004 May;50(5):1412-9.
5 / Xavier Mariette. SFR 2004.
6 / Norihiro Nishimoto Kazuyuki Yoshizaki and all Treatment of rheumatoid arthritis with humanized anti-interleukin-6 receptor antibody: A multicenter double-blind placebo-controlled trial. Arthritis Rheum 2004; 50: 1761-1769.
7 / Larry W. Moreland Rieke Alten Filip Van Den Bosch Thierry Appelboom Marc Leon Paul Emery Stanley Cohen Michael Luggen William Shergy Isaac Nuamah Jean-Claude Becker Costimulatory blockade in patients with rheumatoid arthritis: A pilot dose-finding double-blind placebo-controlled clinical trial evaluating CTLA-4Ig and LEA29Y eighty-five days after the first infusion Arthrith Rheum 2002; 46: 1470-1479. 8 / Joel M. Kremer Rene Westhovens Marc Leon Treatment of Rheumatoid Arthritis by Selective Inhibition of T-Cell Activation with Fusion Protein CTLA4Ig. N Engl J Med 2003;349:1907-15.
Articles les plus lus
- L'arthrose cervicale
- L'arthrose lombaire
- La spondylarthrite ankylosante
- Coxarthrose
- La fibromyalgie
- Les anti-inflammatoires non stéroïdiens. Modalités de prescription.
- Apport de l’échographie dans le diagnostic d’une épaule douloureuse.
- La gonarthrose
- Diagnostic précoce de la polyarthrite rhumatoïde
- La maladie de Behçet



